Con la llegada de la ciencia experimental en los siglos XVI y XVII (véase química), los avances en la teoría atómica se hicieron más rápidos. Los químicos se dieron cuenta muy pronto de que todos los líquidos, gases y sólidos pueden descomponerse en sus constituyentes últimos, o elementos. Por ejemplo, se descubrió que la sal se componía de dos elementos diferentes, el sodio y el cloro, ligados en una unión íntima conocida como compuesto químico. El aire, en cambio, resultó ser una mezcla de los gases nitrógeno y oxígeno.
MODELOS ATOMICOS
| Año | Científico | Descubrimientos experimentales | Modelo atómico | ||||||
| 1808 |  John Dalton |
|
| ||||||
| 1897 |  J.J. Thomson |
|
| ||||||
| 1911 |  E. Rutherford |
|
| ||||||
| 1913 |  Niels Bohr |
|
| ||||||
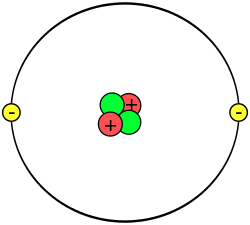
Los átomos son las partículas mas pequeñas de la materia, suelen tener este aspecto, (por supuesto visto a cámara microscópica electrónica)

están formados por partículas subatómicas como por ejemplo protones, los cuales se encuentran justo en el núcleo del átomo junto a LOS NEUTRONES (los protones son partículas de carga positiva), en cambio los neutrones son partículas de carga neutra (es decir 0)
http://www.youtube.com/watch?feature=player_embedded&v=7rXiaZEfyesElectrones

Partículas subatómicas de carga negativa (es decir -) los cuales orbitan alrededor del núcleo.
La mayor parte de la masa del átomo viene del núcleo, donde se hallan los protones y neutrones. También contribuyen en una pequeña parte la masa de los electrones (aunque ella es bastante diría yo mínima)
Los átomos se clasifican de acuerdo al número de protones y neutrones que contenga su núcleo. El número de protones o número atómico determina su elemento químico, y el número de neutrones determina su isótopo. Un átomo con el mismo número de protones que de electrones es eléctricamente neutro. Si por el contrario posee un exceso de protones o de electrones, su carga neta es positiva o negativa, y se denomina ion. (en parte mis favoritos ¡xd¡)
en definitiva todos los átomos son clasificados según su numero de masa electrones, etc. Generalmente son clasificados en una tabla ampliamente conocida por tod@s. (imagen abajo)

(Observaciones: confesaré que las imágenes nos son creaciones propias, por lo que respetare su autoría, en breve dicho copiar y pegar amigos. Lo demás del texto si es mio.)
pinchen el link para mas info es un vídeo
https://www.youtube.com/watch?v=_UizPmivhII
Una partícula subatómica es una partícula más pequeña que el átomo. Puede ser una partícula elemental o una compuesta, a su vez, por otras partículas subatómicas, como son los quarks, que componen los protones y neutrones. No obstante, existen otras partículas subatómicas, tanto compuestas como elementales, que no son parte del átomo, como es el caso de los neutrinos y bosones.
La mayoría de las partículas elementales que se han descubierto y estudiado no pueden encontrarse en condiciones normales en la Tierra, generalmente porque son inestables (se descomponen en partículas ya conocidas), o bien, son difíciles de producir de todas maneras. Estas partículas, tanto estables como inestables, se producen al azar por la acción de los rayos cósmicos al chocar con átomos de la atmósfera, y en los procesos que se dan en los aceleradores de partículas, los cuales imitan un proceso similar al primero, pero en condiciones controladas. De esta manera, se han descubierto docenas de partículas subatómicas, y se teorizan cientos de otras más. Ejemplos de partícula teórica es el gravitón; sin embargo, esta y muchas otras no han sido observadas en aceleradores de partículas modernos, ni en condiciones naturales en la atmósfera (por la acción de rayos cósmicos).
Como partículas subatómicas, se clasifican también las partículas virtuales, que son partículas que representan un paso intermedio en la desintegración de una partícula inestable, y por tanto, duran muy poco tiempo.
PINCHEN EN EL ENLACE ES UN BUEN REPORTAJE
http://www.youtube.com/watch?v=_UizPmivhII
Cuando se descubrió el átomo, se creía que era la unidad mínima más diminuta que existía. Pero observaron mejor el átomo y descubrieron que había cuerpos más pequeños, sus componentes:
*Protones: Componentes del átomo que contiene energía positiva.
*Neutrones: Componentes del átomo que contiene una cantidad equilibrada de energía positiva y negativa.
*Electrones: Componentes del átomo que contienen energía negativa.
Tipos de átomos
En el universo existen más de cien clases de átomos, los cuales suelen unirse para dar origen a distintos tipos de moléculas.
CLASIFICACIÓN DE LOS ELEMENTOS
Clasificamos los enlaces en tres tipos atendiendo a las propiedades de las sustancias formadas. Podemos predecir el tipo de enlace que se dará entre dos átomos fijándonos en el carácter metálico o no de los elementos que lo forman.
Consideramos como metales (color verde) los que tienen tendencia a perder electrones de la capa de valencia y no metales (color azul) los que tienden a ganarlos.
Esa ganancia o pérdida de electrones será la forma de conseguir la estabilidad de una capa completa.
Nos quedarían los semimetales (color rojo) con ambos posibles comportamientos.
Finalmente encontramos los gases nobles (color amarillo), que no presentan tendencia a ganar ni a perder electrones.
Historia: modelos atómicos
Desde la Antigüedad, el ser humano se ha cuestionado de qué estaba hecha la materia.
Unos 400 años antes de Cristo, el filósofo griego Demócrito consideró que la materia estaba constituida por pequeñísimas partículas que no podían ser divididas en otras más pequeñas. Por ello, llamó a estas partículas átomos, que en griego quiere decir "indivisible". Demócrito atribuyó a los átomos las cualidades de ser eternos, inmutables e indivisibles.
Sin embargo las ideas de Demócrito sobre la materia no fueron aceptadas por los filósofos de su época y hubieron de transcurrir cerca de 2200 años para que la idea de los átomos fuera tomada de nuevo en consideración.
El átomo es la unidad de materia más pequeña de un elemento químico que mantiene su identidad o sus propiedades, y que no es posible dividir mediante procesos químicos. Está compuesto por un núcleo atómico, en el que se concentra casi toda su masa, rodeado de unanube de electrones. El núcleo está formado por protones, con carga positiva, y neutrones, eléctricamente neutros. Los electrones, cargados negativamente, permanecen ligados a este mediante la fuerza electromagnética.
http://www.youtube.com/watch?v=tfzr7Yjv3-M
LA TABLA PERIÓDICA
La tabla periódica de los elementos clasifica, organiza y distribuye los distintos elementos químicos, conforme a sus propiedades y características; su función principal es establecer un orden específico agrupando elementos.

http://www.youtube.com/watch?v=z_SjCm-Tgjg
LOS ISOTOPOS
Se denominan isotopos a los átomos de un mismo elemento, cuyos núcleos tienen una cantidad diferente de neutrones, y por lo tanto, difieren en masa atómica. La mayoría de los elementos químicos tienen más de un isotopo Solamente 21 elementos (ejemplos: berilio,sodio poseen un solo isotopo natural; en contraste, el estaño es el elemento con más isotopos estables.
Estructura
La teoría aceptada hoy es que el átomo se compone de un núcleo de carga positiva formado por protones y neutrones, en conjunto conocidos como nucleón, alrededor del cual se encuentra una nube de electrones de carga negativa.

Núcleo atómico
El núcleo atómico se encuentra formado por nucleones, los cuales pueden ser de dos formas:
Protones: Partícula de carga eléctrica positiva igual a una carga elemental, y 1,67262 × 10–27 kg y una masa 1837 veces mayor que la del electrón.
Neutrones: Partículas carentes de carga eléctrica y una masa un poco mayor que la del protón (1,67493 × 10–27 kg).
Alrededor del núcleo se encuentran los electrones que son partículas elementales de carga negativa igual a una carga elemental y con una masa de 9,10 × 10–31 kg.
La cantidad de electrones de un átomo en su estado basal es igual a la cantidad de protones que contiene en el núcleo, es decir, al número atómico, por lo que un átomo en estas condiciones tiene una carga eléctrica neta igual a 0.sss
A diferencia de los nucleones, un átomo puede perder o adquirir algunos de sus electrones sin modificar su identidad química, transformándose en un ion, una partícula con carga neta diferente de cero
Se denominan isótopos (del griego: ἴσος isos 'igual, mismo'; τόπος tópos 'lugar') a los átomosde un mismo elemento, cuyos núcleos tienen una cantidad diferente de neutrones, y por lo tanto, difieren enmasa atómica. La mayoría de los elementos químicos tienen más de un isótopo. Solamente 21 elementos (ejemplos: berilio, sodio) poseen un solo isótopo natural; en contraste, el estaño es el elemento con más isótopos estables.
Otros elementos tienen isótopos naturales, pero inestables, como el uranio, cuyos isótopos están constantemente degradándose, lo que los hace radiactivos. Los isótopos inestables son útiles para estimar la edad de variedad de muestras naturales, como rocas y materia orgánica. Esto es posible, siempre y cuando, se conozca el ritmo promedio de desintegración de determinado isótopo, en relación a los que ya han decaído. Gracias a este método de datación, se conoce la edad de la tierra. Los rayos cósmicos hacen inestables a isótopos estables de Carbono que posteriormente se adhieren a material biológico, permitiendo así estimar la edad aproximada de huesos, telas, maderas, cabello, etc. Se obtiene la edad de la muestra, no la del propio isótopo, ya que se tienen en cuenta también los isótopos que se han desintegrado en la misma muestra. Se sabe el número de isótopos desintegrados con bastante precisión, ya que no pudieron haber sido parte del sistema biológico a menos que hubieran sido aún estables cuando fueron raros.

.gif)


IONES
Un ion1 ("yendo", en griego; ἰών [ion] es el participio presente del verbo ienai: ‘ir’) es unasubpartícula cargada eléctricamente constituida por un átomo o molécula que no es eléctricamente neutra. Conceptualmente esto se puede entender como que, a partir de un estado neutro de un átomo o partícula, se han ganado o perdido electrones; este fenómeno se conoce como ionización.
Los iones cargados negativamente, producidos por haber más electrones que protones, se conocen como aniones (que son atraídos por el ánodo) y los cargados positivamente, consecuencia de una pérdida de electrones, se conocen como cationes (los que son atraídos por el cátodo).
Anión y catión significan:
Anión ("el que va hacia abajo") tiene carga eléctrica negativa.
Catión ("el que va hacia arriba") tiene carga eléctrica positiva.
Ánodo y cátodo utilizan el sufijo '-odo', del griego odos (-οδος), que significa camino o vía.
Ánodo: ("camino ascendente de la corriente eléctrica") polo positivo".2
Cátodo: ("camino descendente de la corriente eléctrica") polo negativo
Los iones cargados negativamente, producidos por haber más electrones que protones, se conocen como aniones (que son atraídos por el ánodo) y los cargados positivamente, consecuencia de una pérdida de electrones, se conocen como cationes (los que son atraídos por el cátodo).
Anión y catión significan:
Anión ("el que va hacia abajo") tiene carga eléctrica negativa.
Catión ("el que va hacia arriba") tiene carga eléctrica positiva.
Ánodo y cátodo utilizan el sufijo '-odo', del griego odos (-οδος), que significa camino o vía.
Ánodo: ("camino ascendente de la corriente eléctrica") polo positivo".2
Cátodo: ("camino descendente de la corriente eléctrica") polo negativo

ENERGIA
1.- Energía y cambio
Al mirar a nuestro alrededor se observa que todo está en continua transformación: en la naturaleza ocurren inmumerables cambios físicos y químicos, la tierra sufre cambios geológicos espectaculares como terremotos y erupciones volcánicas, los seres vivos están en continua actividad, y las máquinas y herramientas realizan las más variadas tareas. Todas estas actividades tienen en común que precisan del concurso de la energía.
La energía es una propiedad asociada a los objetos y sustancias y se manifiesta en las transformaciones que ocurren en la naturaleza.
La energía se manifiesta en los cambios físicos, por ejemplo, al elevar un objeto, transportarlo, deformarlo o calentarlo.
La energía está presente también en los cambios químicos, como al quemar un trozo de madera o en la descomposición de agua mediante la corriente eléctrica.

Cada vez que ocurre un cambio de los mencionados anteriormente, existe una transferencia de energía entre los cuerpos. Existen tres modos principales de transferencia de energía:
2.1.- Trabajo
El Trabajo es una de las formas de transmisión de energía entre los cuerpos. Para realizar un trabajo es preciso ejercer una fuerza sobre un cuerpo y que éste se desplace.
El trabajo, W, de una fuerza aplicada a un cuerpo es igual al componente de la fuerza en la dirección del movimiento, Fx, por el desplazamiento, s, del cuerpo.
W = Fx·s
El trabajo, W, al igual que la energía, se mide en julios (J).
La Potencia es una magnitud que relaciona el trabajo realizado y el tiempo empleado. La potencia mide la rapidez con que se efectúa un trabajo, es decir, la rapidez con que tiene lugar la transferencia de energía desde un cuerpo a otro. Se mide en vatios (W) en el Sistema Internacional.
Los cuerpos emiten energía en forma de radiación. Esta radiación se emite en forma de ondas electromagnéticas como la luz visible, las ondas de radio, los rayos ultravioleta (UV), los rayos infrarrojo (IR), etc. La característica principal de esta energía es que se puede propagar en el vacío, sin necesidad de soporte material alguno.
Al conjunto de radiaciones electromagnéticas se denomina espectro electromagnético. Los diferentes tipos de onda se distinguen por su longitud. A menor longitud de onda, poseen más energía. En orden decreciente de energía se distinguen los rayos gamma, los rayos X, la radiación ultravioleta, la luz visible, la radiación infrarroja, las microondas y las ondas de radio.
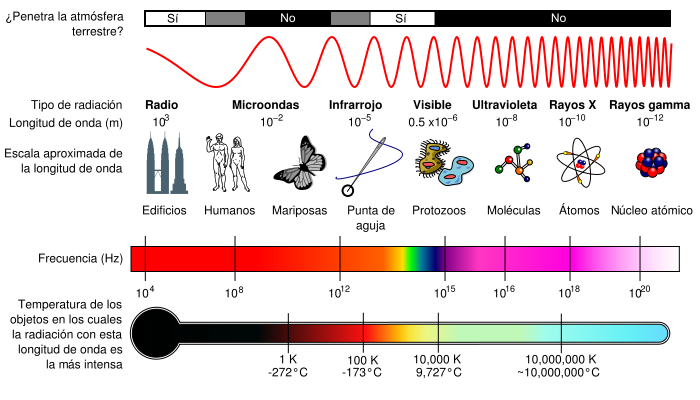
El sol es una estrella que emite gran cantidad de radiación en las diversas longitudes de onda. Las radiaciones más energéticas (rayos gamma, X y ultravioletas), dañinas para los seres vivos, se filtran en la atmósfera y no llegan hasta nosotros. La luz visible es otra parte del espectro de las radiaciones electromagnéticas; nuestros ojos son capaces de detectarlas y de esa manera podemos ver. Los diversos colores corresponden a diferentes longitudes de onda dentro del rango de la luz visible.
Unas formas de energía pueden transformarse en otras. En estas transformaciones la energía se degrada, pierde calidad. En toda transformación, parte de la energía se convierte en calor o energía calorífica.
Cualquier tipo de energía puede transformarse íntegramente en calor; pero, éste no puede transformarse íntegramente en otro tipo de energía. Se dice, entonces, que el calor es una forma degradada de energía.
Por ejemplo:
- La energía eléctrica, al pasar por una resistencia, produce calor (por eso se calientan las bombillas).
- En la combustión de algunas sustancias, parte de la energía química se convierte en calor (por eso el fuego calienta).
- Las máquinas, como los coches, se calientan cuando están en marcha porque parte de su energía se transforma en calor.
3.- Formas de Energía
Existen diferentes formas de energía. Por su naturaleza se pueden distinguir la energía potencial y la energía cinética.
A) La energía potencial es la energía contenida en un cuerpo, por ejemplo: la energía humana, la del agua, del vapor, etc.
a.1- La energía potencial gravitatoria se define como la energía determinada por la posición de los cuerpos. Esta energía depende de la altura y el peso del cuerpo según la ecuación:
Ep = m . g . h = Peso . h (un cuerpo de masa m situado a una altura h posee energía).
a.2.- Otra forma común de energía potencial es la que posee un cuerpo elástico cuando se comprime, se estira o se deforma, pues tiene capacidad para recuperar su posición original: es la energía potencial elástica. Por ejemplo, un arco tensado tiene energía potencial elástica.

B) La energía cinética es la que posee un cuerpo debido a su movimiento o velocidad; por ejemplo: la energía del agua al caer de una cascada, la energía del aire en movimiento, o la de la flecha impulsada por el arco. Ésta energía depende de la masa y de la velocidad según la ecuación:
Ec = ½ m . v2 (Un cuerpo de masa m que lleva una velocidad v posee energía).
Existen también otras clasificaciones de la energía que en su esencia son energía cinética o potencial o combinaciones de estas dos:
Energía Calórica o térmica: Producida por el aumento de la temperatura de los objetos. Como sabemos, los cuerpos están formados por moléculas y éstas están en constante movimiento. Cuando aceleramos este movimiento se origina mayor temperatura y al haber mayor temperatura hay energía calorífica. Esto es lo que sucede cuando calentamos agua hasta hervir y se produce gran cantidad de vapor.
Energía Mecánica: Es la capacidad que tiene un cuerpo o conjunto de cuerpos de realizar movimiento, debido a su energía potencial o cinética; por ejemplo: La energía que poseemos para montar en bicicleta (energía potencial) y hacer cierto recorrido (energía cinética); o el agua de unas cascada (energía potencial por estar a una altura y cinética porque se mueve).

Energía Química: Es la producida por reacciones químicas que desprenden calor o que por su violencia pueden desarrollar algún trabajo o movimiento. Los alimentos son un ejemplo de energía química ya que al ser procesados por el organismo nos ofrecen calor (calorías) o son fuentes de energía natural (proteínas y vitaminas) . Los combustibles al ser quemados producen reacciones químicas violentas que producen trabajo o movimiento.

Energía Eléctrica: Es la debida al movimiento de electrones, por lo que es una forma de energía cinética. Esta una forma energía muy conocida y utilizada por todos; la utilizamos diariamente en nuestros hogares para hacer funcionar nuestros electrodomésticos, y en otros aspectos de la vida para hacer funcionar todo tipo de máquinas y producir luz.
Aún existen muchas otras formas de energía que tienen gran aplicación práctica en la industria como: La nuclear, la energía radiante, etc.
3.- Conservación y degradación de energía
Hemos visto que la energía se encuentra en constante transformación, pasando de unas formas a otras. ¿Qué ocurre con la cantidad total de energía en esos cambios?
El Principio de conservación de la energía indica que la energía no se crea ni se destruye; sólo se transforma de unas formas en otras. En estas transformaciones, la energía total permanece constante; es decir, la energía total es la misma antes y después de cada transformación.
Sin embargo, en toda transformación, parte de la energía se convierte en calor o energía calorífica. Por ello, se dice que la energía se degrada, ya que, como hemos visto anteriormente, el calor es una forma degradada de energía.
Tomemos como ejemplo la siguiente ilustración del patinador que se desliza por la pista de skate:

- La energía mecánica del patinador se está transformando constantemente de energía potencial (energía debida a la altura en que está) a cinética (energía debida a la velocidad que lleva). En los bordes, la enegía potencial es máxima y la cinética mínima; en el centro ocurre lo contrario. Pero en cada punto, la suma de las dos energías es constante (conforme disminuye una, aumenta la otra). Si esto fuera así, el patinador nunca pararía si no frenase. En la realidad, sabemos que irá perdiendo paulatinamente velocidad y altura, hasta acabar en el centro. Esto se debe a que el rozamiento del patinete con el suelo va disipando parte de la energía en forma de calor, y finalmente, si el patinador no se impulsa, el sistema perderá toda su energía mecánica y se detendrá




El ser humano, como ser vivo que es, necesita energía para vivir y realizar sus actividades. Conforme nuestra especie ha ido desarrollándose cultural y tecnológicamente, las necesidades y el consumo de energía han ido aumentando.
El fuego fue nuestra primera gran fuente de energía: quemando madera, transformábamos la energía química de la propia madera en luz y calor. Gracias a ello, pudieron transformarse los alimentos para digerirlos más fácilmente, y se crearon nuevas herramientas y aparatos.
A lo largo de la historia, el hombre ha aprovechado diversos recursos naturales, (viento, agua, carbón, luz solar, etc) para realizar actividades cada vez más complejas.
Hoy en día, vivimos en una sociedad muy desarrollada tecnológicamente, lo que implica que tenemos una gran necesidad de energía para que todos nuestros aparatos funcionen. Consecuentemente, el consumo de energía se ha disparado en las últimas décadas.
Tal necesidad de energía ha hecho que busquemos constantemente recursos a partir de los cuales obtener energía. A estos recursos se les denomina fuentes de energía.
3.1.- Fuentes de energía
Las fuentes de energía son los recursos existentes en la naturaleza de los que la humanidad puede obtener energía utilizable en sus actividades.
El origen de casi todas las fuentes de energía es el Sol, que "recarga los depósitos de energía". Las fuentes de energía se clasifican en dos grandes grupos: renovables y no renovables; según sean recursos "ilimitados" o "limitados".
3.1.1- Energías renovables
Las Fuentes de energía renovables son aquellas que, tras ser utilizadas, se pueden regenerar de manera natural o artificial. Algunas de estas fuentes renovables están sometidas a ciclos que se mantienen de forma más o menos constante en la naturaleza.
Las principales fuentes de energía renovables son:
· La energía mareomotriz es la producida por el movimiento de las masas de agua provocado por las las mareas, o por las olas que se originan en la superficie del mar por la acción del viento.

A pesar de que no genera residuos y es casi inagotable, no abundan los sitios idóneos para tales instalaciones, que además son grandes y costosas.

· La energía hidráulica es la producida por el agua retenida en embalses o pantanos a gran altura (que posee energía potencial gravitatoria). Si en un momento dado se deja caer hasta un nivel inferior, esta energía se convierte en energía cinética y, posteriormente, en energía eléctrica en la central hidroeléctrica.

Es una fuente de energía limpia, sin residuos y fácil de almacenar, pero la construcción de centrales hidroeléctricas es costosa. Además, los embalses provocan importantes impactos ambientales, bien porque inundan valles enteros,
| · La energía eólica es la energía cinética producida por el viento. Tradicionalmente aprovechada mediante molinos de viento, hoy en día se transforma en electricidad en unos aparatos llamados aerogeneradores. Es una fuente de energía limpia e inagotable, y aunque las instalaciones son caras, el mantenimiento tiene bajo coste. No obstante, es irregular, pues depende de la fuerza del viento, y además su instalación puede cusar importantes impactos ambientales sobre el paisaje y la fauna. · La energía geotérmica es aquella que puede ser obtenida mediante el aprovechamiento del calor del interior de la Tierra, generalmente para producir electricidad, pero tanbién agua caliente. Aunque no abundan los sitios idóneos, es una fuente de energía casi inagotable y muy rentable.  · La energía solar, generada en el Sol por fusión nuclear, llega a la Tierra en forma de radiación electromagnética. El aprovechamiento de esta energía se puede realizar de dos formas: - Mediante la conversión térmica se transforma la energía solar en energía térmica almacenada en un líquido (por ejemplo agua).  - Mediante la conversión fotovoltaica se transforma la energía luminosa en energía eléctrica. Se utilizan para ello unas placas solares formadas por células fotovoltaicas (de silicio o de germanio).  Es una fuente de energía no contaminante, barata e inagotable, pero su rendimiento es bajo, y depende mucho del clima. · La energía de la biomasa es la que se obtiene de la materia orgánica mediante procesos naturales. Es una fuente de energía usada desde muy antiguo (la leña, el estiércol o restos de cultivos se han usado tradicionalmente para hacer fuego). Hoy en día, además de la combustión directa, se utiliza esa materia para transformarla en otros combustibles, como alcohol, metanol, aceite, biogás, biodiesel, etc.  Es una fuente de energía limpia que permite aprovechar residuos de la actividad humana, pero también puede suponer la hipoteca de terrenos agrícolas que se destinan a obtener productos para este fin, y además indirectamente hacen subir el precio de ciertos alimentos. 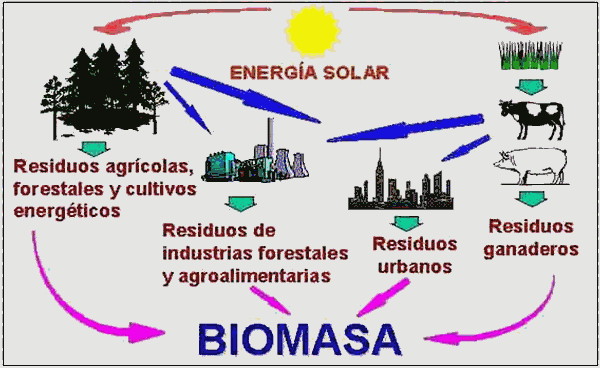 Las fuentes de energía no renovables son aquellas que se encuentran de forma limitada en el planeta y cuya velocidad de consumo es mayor que la de su regeneración. Las energías no renovables se dividen en dos grandes prupos: · Los combustibles fósiles (carbón, petróleo y gas natural) son sustancias originadas por la acumulación, hace millones de años, de grandes cantidades de restos de seres vivos en el fondo de lagos y otras cuencas sedimentarias. Son relativamente fáciles de obtener y tienen un gran rendimiento energético, razón por la que son muy utilizadas hoy en día. Pero, además de ser contaminantes, se agotarán en un plazo relativamente corto. El carbón se utiliza como combustible en la industria, en las centrales térmicas y en las calefacciones domésticas.  El petróleo tiene, hoy día, muchísimas aplicaciones, entre ellas: gasolinas, gasóleo, abonos, plásticos, explosivos, medicamentos, colorantes, fibras sintéticas, etc. Además, se emplea en las centrales térmicas como combustible.  El gas natural tiene un origen similar al del petróleo y suele estar formando una capa o bolsa sobre los yacimientos de petróleo. Está compuesto, fundamentalmente, por metano (CH4). Tiene aplicaciones parecidas a las del carbón.  · La Energía nuclear es la energía almacenada en el núcleo de los átomos, que se desprende en la desintegración de dichos núcleos.  La energía nuclear de fisión se obtiene al bombardear, con neutrones a gran velocidad, los átomos de ciertas sustancias pesadas radiactivas(uranio, plutonio); algunos de estos neutrones alcanzan el núcleo atómico y lo rompen en dos partes. Se libera una gran cantidad de energía y algunos neutrones. Estos neutrones pueden chocar contra otros núcleos, que se romperán produciendo más energía y más neutrones que chocarán contra otros núcleos. Esto es una reacción en cadena. En estas reacciones, una pequeña parte de masa se transforma en energía (según la ecuación E = mc2 de Einstein), y se obtiene un rendimiento energético extraordinario. Así, en las centrales nucleares se aprovecha esta energía para producir electricidad. De esta manera, pequeñas cantidades de combustible producen mucha energía, pero se generan residuos radiactivosde difícil eliminación. Además, las centrales nucleares son susceptibles de tener fallos de graves consecuencias, por lo que tienen sistemas de seguridad muy costosos.  Una alternativa ideal es la energía nuclear de fusión, la reacción que produce la energía en las estrellas. En la fusión nuclear se unen átomos pequeños como el hidrógeno (abundante en la naturaleza) para formar otros de mayor tamaño como el helio, y no se producen residuos radiactivos. El problema es que para que esta reacción se desencadene hace falta una temperatura de 100 millones de grados centígrados, algo muy difícil y costoso de conseguir. Con la tecnología actual, se necesitaría gastar más energía en conseguir esa temperatura que la que se obtendría en el proceso. Esquema de una reacción nuclear de fusión: liberándose mucha energía. 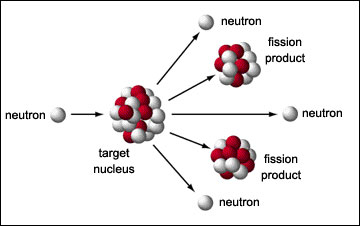  Espero que les haya gustado mi blog, y porsupuesto si pueden ayudarme con el blog les rogaría que visiten estas URlS (hace referencia a Poquet Price Comercial españa) Click aqui para ayudar la URL: Clik para ayudar http://adf.ly/1A53ch con ello por solo 5 segundos me aportaran unos pocos centimos. porsupuesto no me los pagan vosotros sino la empresa de publicidad. Gracias amigos. |